金属水素化物MgH2不安定化の第一原理計算: 添加剤による水素放出促進効果#

金属水素化物(代表例:MgH2)は、高密度に水素を貯蔵できる材料として期待されていますが、非常に安定であるという課題があります。MgH2から水素(H2)を取り出すためには250℃以上といった高温が必要であり、実用化の大きな障壁となっています。そこで、より低い温度でH2を放出させるための「不安定化(Destabilization)」技術が求められています。本解析では、第一原理計算ソフトウェアAdvance/PHASEを用い、添加剤(Si)がMgH2の水素放出エンタルピー(ΔH)をどれだけ低減できるか(不安定化できるか)を定量的に評価します。
Keywords: 第一原理計算, DFTシミュレーション, 水素貯蔵材料, 金属水素化物, MgH2, 不安定化, 添加剤, 反応エンタルピー
計算方法#
添加剤(Si)の効果を明確にするため、「添加剤なし」の基準反応と「Si添加」の不安定化反応の2つのエンタルピー(ΔH)を直接比較します。
A. 基準反応(添加剤なし)#
MgH2が分解し、金属Mgと水素H2になる基本的な反応です。この反応エンタルピーΔHAが、材料の実用性を判断する基準となります。
B. 不安定化反応(Si 添加)#
あらかじめMgH2と添加剤Siを混合しておく系を想定します。H2放出後、残ったMgがSiと即座に反応し、非常に安定な化合物である Mg2Si を形成します。この「安定な受け皿」が形成されることにより、系全体としてH2を放出しやすくなる(=不安定化する)と考えられます。
エンタルピー(ΔH)の算出#
各反応のエンタルピー(ΔH)は、各物質の全エネルギー(E)から以下のように算出します。
注記:ZPE(ゼロ点エネルギー)補正の省略について
本解析では、2つの反応(AとB)の「差」を比較することが目的であるため、ZPE補正を省略しています。これは、以下の理由に基づいています。
- 反応エンタルピーのZPE補正(ΔZPE)は、「生成物のZPE合計」から「反応物のZPE合計」を引いた値であり、その寄与は主に軽い原子(H)の振動に由来します。
- 両反応(A, B)とも、「固体中のH(in MgH2)」が「気体中のH(in H2)」に変わる点が、ΔZPEの最大の寄与項となります。H2 1モルあたりで比較すると、これは両反応の共通項です。
- したがって、H2 1モルあたりのZPE補正の差( と の差)は、残りの重い原子のみで構成される固体(Mg, Si, Mg2Si)のZPEの差に起因します。
- これらの重い原子が関わるZPEの差は、Hが関わる上記の大きな共通項に比べて十分に小さいため、無視できるとみなせます。
- その結果(共通項はほぼ等しく、差分の要因は無視できるため)、 と近似することができます。
したがって、不安定化の効果()は、ZPE補正を行わない0Kの全エネルギー比較で十分に議論可能であると判断しました。
計算モデルと計算条件#
DFT計算にはMgH2(正方晶構造、P42/mnm対称性)、Mg2Si(立方晶構造、Fm3m対称性)、Si(diamond構造)、Mg(六方晶HCP構造) の各結晶モデル、およびH2分子モデルを使用しました。
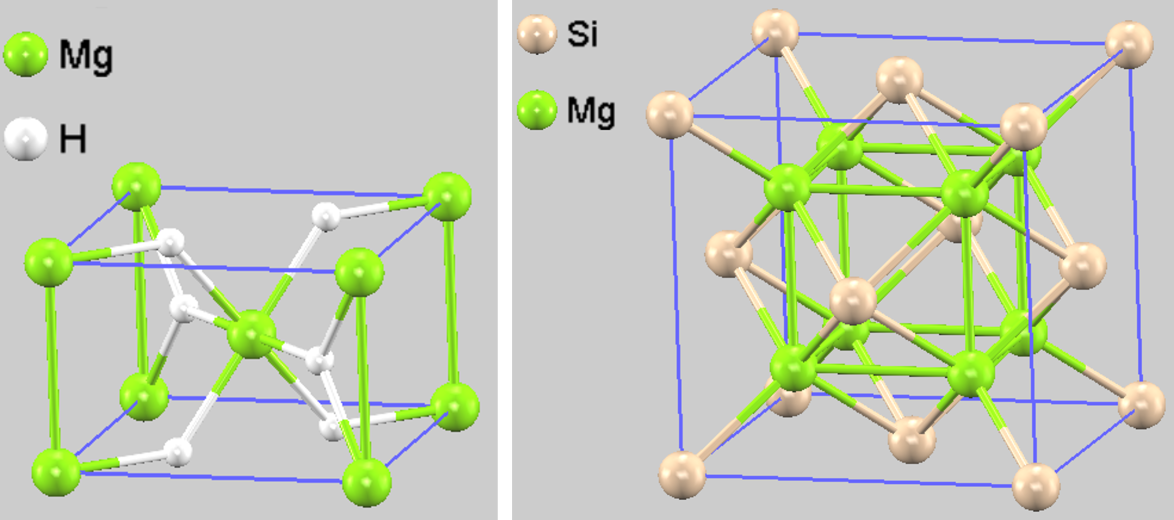
図1. 計算に用いた (左) MgH2 と (右) Mg2Si の計算セル
本解析で用いた主な計算条件は表1に示されています。
表1. 計算条件の概要
| 項目 | 設定 |
|---|---|
| 擬ポテンシャル | PAWポテンシャル |
| 交換相関汎関数 | GGA (PBE) |
| 波動関数のカットオフエネルギー | 25 Rydberg |
| k点サンプリング | セルサイズや金属性有無に応じて十分に設定 |
計算結果と考察#
最適化された格子定数#
MgH2とMg2Siの構造(図1)を最適化し、格子定数を算出しました。表2に示すように、本計算値(PBE)は実験値 [1] と文献値 (GGA-PW91を用いた計算値)[2] と良好な一致を示しており、計算の妥当性が確認できます。
表2. MgH2とMg2Siの最適化した格子定数 (単位: Å)
| 物質 | 項目 | 計算値 (PBE) | 文献値(PW91) | 実験値 |
|---|---|---|---|---|
| MgH2 | a | 4.522 | 4.466 | 4.517 |
| MgH2 | c | 3.022 | 2.992 | 3.021 |
| Mg2Si | a | 6.360 | 6.361 | 6.390 |
水素放出エンタルピー#
次に、2つの反応のエンタルピー(ΔH)を算出しました。表3に示す値は、基準反応(A)と不安定化反応(B)を比較するため、すべてH2 1モルあたりの放出エンタルピー(単位: kJ/(mol H2)、もしくはkJ/mol H2)として正規化しています。
表3. 水素放出エンタルピー(ΔH)の比較 (単位: kJ/mol H2)
| 反応 | 本計算 (PBE) | 文献値 (PBE) | 文献値 (PW91) | 実験値 [1] |
|---|---|---|---|---|
| A. 基準反応 (MgH2 → Mg + H2) | 55.64 | 55.3 | 65.1 | 70.6 |
| B. 不安定化反応 (2MgH2 + Si → ...) | 31.89 | 31.4 | 37.9 | - |
考察#
基準反応(A)のエンタルピーは 55.64 kJ/mol H2 であり、これは水素放出のためには高温を必要とする、比較的高い値です。一方、Si を添加した不安定化反応(B)では、エンタルピーが 31.89 kJ/mol H2 へと劇的に低下しました。この結果は、H2放出後に残ったMgがSiと反応して Mg2Si という非常に安定な化合物を形成することで、H2放出が熱力学的に有利になる(不安定化する)という概念を明確に裏付けています。本計算で用いたPBE汎関数による計算値は、文献 [2] のPBE計算値と非常によく一致しています。汎関数の種類(PBEとPW91)によってΔHの絶対値は異なりますが、Siの添加によって水素放出エンタルピーが大幅に低下するという物理的な傾向は、VajoらによるSi添加系での実験報告 [3] とも整合的であり、添加剤による不安定化効果の妥当性を示しています。
まとめ#
本解析では、第一原理計算ソフトウェアAdvance/PHASEを用い、金属水素化物MgH2の水素放出エンタルピーに対する添加剤(Si)の効果を評価しました。計算の結果、添加剤なしの基準反応 (MgH2 → Mg + H2) のエンタルピーが 55.64 kJ/mol H2 であるのに対し、Si を添加した不安定化反応 (2MgH2 + Si → Mg2Si + 2H2) では 31.89 kJ/mol H2 へと大幅に低下することが示されました。これは、Siを添加することで H2 放出後に安定な Mg2Si が生成されるため、熱力学的に水素が放出されやすくなる(不安定化する)ことを定量的に示しており、第一原理計算が水素貯蔵材料の設計において強力なツールであることを示しています。
本解析の詳細や、研究への適用可能性に関するご相談はこちら
お問い合わせ参考文献#
- D. R. Lide (Ed.), CRC Handbook of Chemistry and Physics, 83rd ed., CRC Press, New York, 2002.
- S. V. Alapati, J. K. Johnson, and D. S. Sholl, "Identification of destabilized metal hydrides for hydrogen storage using first principles calculations", J. Phys. Chem. B 110, 8769 (2006).
- J. J. Vajo, F. Mertens, C. C. Ahn, R. C. Bowman, Jr., and B. Fultz, "Altering Hydrogen Storage Properties by Hydride Destabilization through Alloy Formation: LiH and MgH2 Destabilized with Si", J. Phys. Chem. B 108, 13977 (2004).
関連ページ#
- 第一原理計算ソフトウェア Advance/PHASE
- 解析分野:ナノ・バイオ
- 産業分野:材料・化学